Як уникнути мікотоксинів у зерні: нові відкриття про поведінку грибів
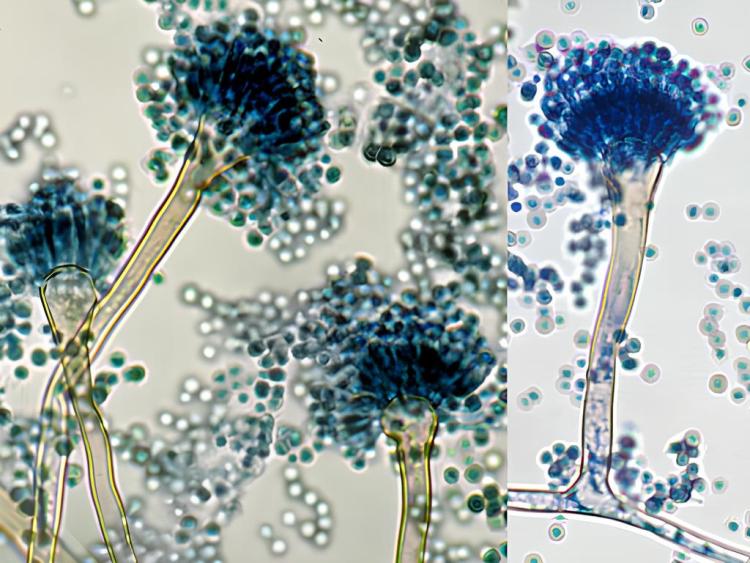
Конідії Aspergillus flavus (Афлатоксин B1)
Понад 25% світового врожаю щороку уражається токсигенними грибами. Сукупні втрати продовольства наближаються до 1,3 млрд тонн на рік — майже третина глобального виробництва їжі. Економічний збиток поглиблюється тим, що мікотоксини є термостабільними вторинними метаболітами, які не інактивуються стандартними технологічними операціями: помолом, хлібопеченням, екструзією або пресуванням олії.
Проблема контамінації зерна мікотоксинами є особливо актуальною для України. У 2022 та 2025 роках внаслідок підвищеної вологості під час збирання кукурудзи фіксувалися випадки перевищення гранично допустимих рівнів мікотоксинів, зокрема DON, ZEN та фумонізинів, що створювало суттєві ризики втрати експортної якості зерна. Зерно кукурудзи, залишене на перезимівлю в полі або зібране за підвищеної вологості (>25%) без подальшого доведення до стандартних параметрів зберігання шляхом сушіння, формує сприятливе середовище для розвитку грибів родів Fusarium та Aspergillus.
Мікотоксини потрапляють у харчовий ланцюг у результаті ураження сільськогосподарських культур пліснявими грибами як у період вегетації, так і під час зберігання та після збирання врожаю. Синтезовані ними токсичні сполуки характеризуються високою термостабільністю та практично не руйнуються в процесі технологічної переробки сировини, зокрема під час виробництва борошна, випікання хліба, виготовлення рослинної олії чи комбікормів. Унаслідок цього можливе їх безпосереднє потрапляння до харчових продуктів, формуючи потенційний шлях контамінації за принципом «від поля до столу».

Окрім прямого надходження через рослинну продукцію, мікотоксини можуть потрапляти до організму людини опосередковано — через продукцію тваринництва (молоко, м’ясо, яйця), у якій вони здатні акумулюватися. Тривалий вплив цих токсичних сполук пов’язують із розвитком низки патологічних станів, зокрема онкологічних, імунних та ендокринних порушень.
Водночас в Україні досі відсутня цілісна система державного моніторингу мікотоксинів у зерновій продукції. Натомість у більшості країн-імпортерів українського зерна контроль за вмістом цих токсинів є обов’язковим і здійснюється відповідно до жорстких регуляторних вимог.
Проте справжня небезпека сталася не лише в масштабах зараження, а й у тому, що наука і практика досі розглядали кількість основних мікотоксинів як єдину однорідну загрозу. Нова наукова робота доводить: це принципова помилка, що коштує аграріям врожаю, а споживачам — здоров'я.

Мікотоксини на початках кукурудзи
Науковою групою під керівництвом д.б.н. С. Хаблака, виконано ґрунтовне експериментальне дослідження на тему: «Екологічна сегрегація мікотоксигенних патогенів у зерні: двопорогова модель водної активності та температури як предикторів ризику контамінації впродовж харчового ланцюга».
Проблема глибша, ніж здається.
Мікотоксини — афлатоксин B1, охратоксин A, дезоксиніваленол (DON), зеараленон (ZEN), фумонізини та T-2/HT-2 токсини — традиційно об’єднуються в одну категорію загрози зерновому виробництву. Однак детальний аналіз їхніх екологічних параметрів виявляє принципово відмінну картину.
Науковці встановили, що шість основних мікотоксинів у людини формують два екологічно несумісних кластери, визначених двома ключовими параметрами: водною активністю субстрату (Aw) і температурою синтезу токсину. Змішування двох цих груп в єдину стратегію управління ризиком — одна з головних причин неефективності чинних програм моніторингу.
Два типи патогенів — дві точки різних втручань.
У роботі пропонується двопорогова модель ризику, яка чітко розмежовує:
- Тип I — патогени зберігання (Aspergillus/Penicillium ): синтезують афлатоксин В1 та охратоксин А за водної активності ≥0,77–0,78, що відповідає вологості зерна лише 13–15%. Критична фаза ризику — складське зберігання, особливо влітку та на початку осені.
- Тип II — польові патогени (Fusarium spp.): продукують DON, ZEN, фумонізини та T-2/HT-2 токсини лише за Aw ≥0,88–0,90, тобто у вологі зерні або в полі. Критична фаза — збирання та перші тижні після нього.
Практичний наслідок цього розмежування кардинальний: ефективний моніторинг двох різних протоколів, а не єдиної уніфікованої схеми відбору зразків.
Критичне виправлення: оптимальний синтез зеараленону — не 25°C, а 12–15°C.
Одним із центральних результатів роботи є виправлення розширеної в літературі помилки щодо оптимальної температури синтезу зеараленону. У переважній ситуації підручників, агрономічних довідників і консультативних матеріалів зазначається 25°C — значення, яке насправді відповідає оптимальному росту міцелію, а не синтезу токсину. Первинні експериментальні дані однозначно свідчать: справжній оптимальний синтез ZEN становить 12–15°C , а при 37°C синтез повністю припиняється.
Порівняльний аналіз демонструє, що оптимальні температурні умови для росту мікотоксигенних грибів не завжди збігаються з умовами максимального синтезу мікотоксинів. У багатьох випадках продукція токсинів відбувається при нижчих температурах, ніж ті, які сприяють найінтенсивнішому росту міцелію. Це має важливе значення для прогнозування ризику контамінації зерна, особливо за прохолодної та вологої погоди під час дозрівання або зберігання продукції.
З агрономічної точки зору це виправлення є надзвичайно корисним: пшениця і кукурудза, що залишаються в полі протягом липня-серпня та жовтня–листопада-грудня-січня-лютого в Україні та Центральній Європі, накопичують зеараленон із максимально можливою швидкістю саме тоді, коли аграрії вважають осінній і зимовий періоди відносно безпечними. Щотижневі затримки зі збиранням після зниження температури нижче 20 °C суттєво підвищують рівень ZEN у зерні.
Автори наголошують, що всі національні і закордонні настанови та консультативні матеріали щодо управління ризиком ZEN, які вказують 25 °C як оптимальну температуру синтезу, потребують уточнення і перегляду.
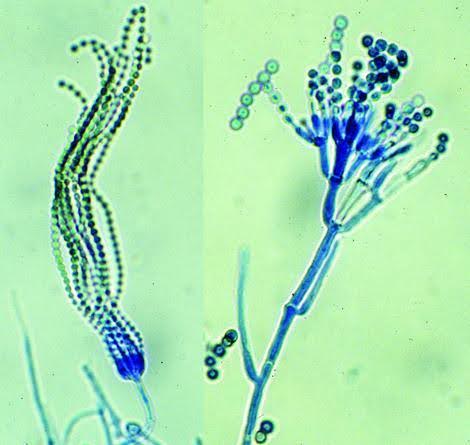
Penicillium Verrucosum (Охратоксин A)
Три сезонних вікна ризику для помірного клімату.
Аналіз виявив три неперекривних вікна небезпеки, характерних для агрокліматичних умов України:
- Тепле зберігання (червень–вересень) — домінує ризик афлатоксину B1 при температурі понад 25°C і вологості зерна від 15%.
- Осіння польова фаза (вересень–листопад) — максимальний ризик ZEN (опт. 12–15°C) та DON (опт. 20–25°C) у недозібраній або вологій кукурудзі.
- Зимові цикли заморожування та відтавання (грудень–березень) створюють унікальні умови для активності токсинів Т-2/НТ-2: синтез цих мікотоксинів підтверджений навіть при температурах до −2 °C. Кукурудза, що залишається в полі взимку, не є «законсервованим» врожаєм, а слугує субстратом, на якому накопичується токсин Т-2, особливо при пошкодженні або деградації зернової оболонки і клітин кристаликами льоду.
Кукурудза — єдина культура з усіма шістьма токсинами одночасно.
У роботі вперше систематизовано матрицю сприйнятливості культури: кукурудза є господарем усіх шести токсинів одночасно. Пшениця уражається чотирма, ячмінь — трьома, овес — двома. Морфологія качана, тривалий налив зерна та підтримка збирання формують унікальний комплекс ризиків, якого не має жодна інша культура.
Від поля — до столу: невидимий шлях.
Термостабільність усіх шести мікотоксинів означає: жоден з них не руйнується при варінні, хлібопеченні, пресуванні олії або виробництві комбікормів. Заражене зерно незворотно контамінує всі похідні продукти. Афлатоксин B1 перетворюється в організмі корів на AFM1 — канцероген групи 1 IARC — і виявляється в молоці. Охратоксин А накопичується в м'язовій тканині свиней і птиці. Зеараленон руйнує гормональну систему тварин задовго до появи клінічних ознак.
Споживач, який ніколи не торкався забрудненого зерна, щодня отримує мікотоксини через м'ясо, молоко та хлібопродукти — непомітно та кумулятивно.
Двопорогова модель як основа нових стандартів моніторингу.
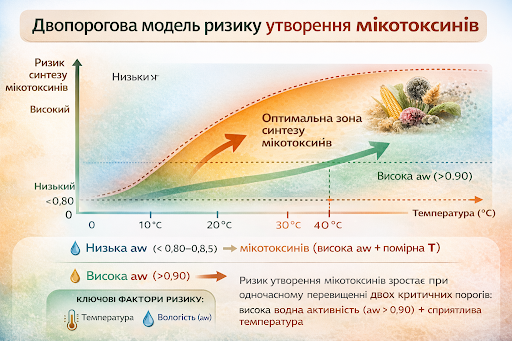
Дослідниками розроблена двопорогова модель ризику утворення мікотоксинів, яка пояснює синтез цих токсичних метаболітів як процес, що визначається двома ключовими факторами середовища: водною активністю (aw) та температурою. Ріст грибів і продукція токсинів майже не відбуваються при aw менше 0,80, тоді як при значеннях від 0,85 до 0,90 можливе обмежене розмноження грибів. Активний синтез мікотоксинів спостерігається при aw, що перевищує 0,90.
Температура середовища виступає другим критичним порогом і визначає тип мікотоксину, що може утворюватися. Так, афлатоксини продукуються переважно при 25–33 °C, DON і ZEN – при 15–25 °C, фумонізини – при 20–30 °C, а токсин T-2 – при 0–15 °C.
Таким чином, основний науковий висновок полягає в тому, що реальний ризик контамінації зерна мікотоксинами виникає лише за одночасного перевищення обох порогів: водної активності ≥ 0,90 та сприятливої температури для конкретного токсину. З огляду на це, контроль вологості зерна після збирання є найефективнішим заходом профілактики утворення мікотоксинів, забезпечуючи суттєве зниження ризику їх накопичення в продукції.
Ключовий практичний висновок роботи: ризик мікотоксинів є цілорічним і не може бути усунений жодним єдиним температурним або вологісним порогом. Автори пропонують прийняти матрицю Aw × температуру як концептуальну основу для стратифікованого за програмою ризику відбору зразків зерна — замість поточних підходів із фіксованою частотою, що ігнорують принципову різницю між польовою та складною фазами накопичення токсинів.
Оскільки всі шість токсинів є термостабільними, єдиною ефективною стратегією залишається профілактична: тимчасове збирання, швидке просушування зерна та збереження умов. Будь-яке запізнення на рівні поля — це незворотне рішення для всього подальшого харчового ланцюга.
Мікотоксини: прихована небезпека
